
에임메드의 인지치료 소프트웨어 ‘솜즈(Somzz)’가 국내 첫 ‘디지털치료기기’로 15일 허가됐다.
‘Somzz’는 불면증 증상 개선을 목적으로 불면증 환자를 치료하는 방법의 하나인 ‘불면증 인지행동 치료법(CBT-I; Cognitive Behavioral Therapy for Insomnia)’ 프로토콜을 모바일 앱으로 구현한 소프트웨어 의료기기다. 불면증을 지속시키거나 악화시키는 심리적·행동적·인지적 요인들에 대한 중재(교정)을 목표로 한다. 만성 불면증에서 약물 치료 이전에 우선적으로 고려돼야 하는 치료방법으로 알려져 있다.
모바일 앱이 제공하는 △수면 습관 교육 △실시간 피드백 △행동 중재 등을 6~9주 간 수행함으로써 수면의 효율을 높여 불면증을 개선하는 원리로 작동된다.
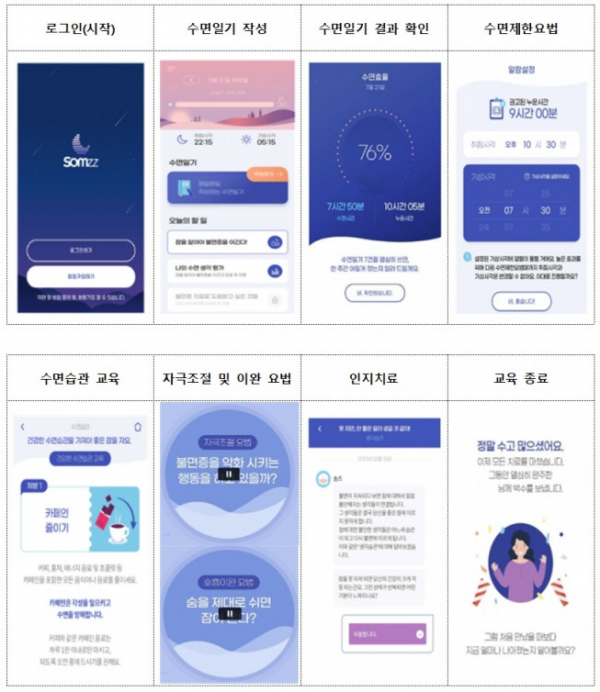
국산 1호 디지털치료기기로 품목허가를 한 식품의약품안전처에 따르면 수면일기 작성→수면일기 결과 확인→수면제한요법→수면습관 교육→자극조절 및 이완 요법→인지치료 등 6단계 프로그램을 6~9주 동안 모두 완료해야 불면증 증상개선 효과를 확인할 수 있다.
해당 제품은 병원에서 진료를 받은 뒤 애플리케이션을 내려받아 사용할 수 있다. 다만, 아직 상용화까지는 갈 길이 멀다. 솜즈는 혁신의료기기로 지정돼 이를 활용하는 병원에서는 이용할 수 있지만, 아직 건강보험 급여 체계에는 포함되지 않았다.
이와 관련 식약처는 적절한 시장 가치를 인정해주고 신속히 시장에 진입할 수 있도록 보건복지부 등 관계부처와 긴밀히 협의할 계획이다.
‘Somzz’는 수면 제한으로 인한 졸음 유발이 직장이나 일상생활에서 심각한 사고를 줄 수 있는 경우에는 사용해선 안 된다. 장거리 트럭 운전사 및 버스 운전기사, 항공교통관제사, 중장비 운전자 등이 해당된다. 또한 수면보행증 및 야경증 등의 사건수면, 간질, 낙상 위험이 높은 개인, 퇴행성 질환이 있는 경우 등도 병태 생리를 악화시킬 수 있어 사용해선 안 된다.
만약 ‘Somzz’를 사용하다 부작용이 발생하는 경우 그 사실을 진료 받은 의료기관 또는 의료기기 제조업자에게 알리거나 식약처의 ‘의료기기 전자민원청구’를 통해 이상사례를 보고해야 한다.
오유경 식약처장은 이날 브리핑에서 “국내에 불면증으로 진단받은 환자가 67만 명에 달한다. 불면증으로 고민하고 있는 잠재적인 사람까지 포함한다면 이 제품으로 수혜 받을 환자는 더 많을 것이라고 전망한다”고 설명했다.
국내 1호 디지털치료기기로 품목허가를 받은 ‘솜즈’에 이어 2호, 3호 디지털치료기기 개발에도 속도가 붙을 전망이다.
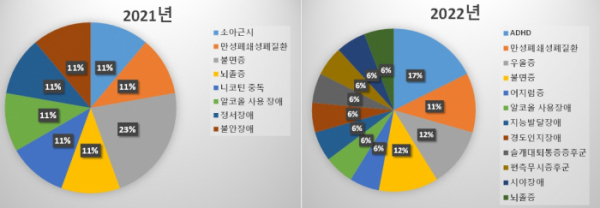
식약처의 ‘디지털치료기기 임상시험 승인현황’에 따르면 2021년 9건의 임상시험계획이 8개 질환에 대해 승인됐고, 지난해에는 17건의 임상시험계획이 12개 질환에 대해 승인된 바 있다. 특히 지난해에는 경도인지장애와 주의역결핍·과잉행동장애(ADHD), 발달장애 등 다양한 질환에 적용이 시도되고 있다.
이에 따라 식약처는 2027년까지 10종의 맞춤형 디지털치료기기 임상·허가 관련 가이드라인을 추가로 개발하는 등 국제적인 규제 글로벌 스탠다드를 선도·충족할 수 있도록 지원을 강화할 계획이다. 식약처에 따르면 현재 불면증 등 5종 회에 올해 ADHD·섭식장애 관련 2종을 개발하고, 2027년까지 8종을 추가할 예정이다.

![잠자던 내 카드 포인트, ‘어카운트인포’로 쉽게 조회하고 현금화까지 [경제한줌]](https://img.etoday.co.kr/crop/140/88/2100528.jpg)
!['20년 째 공회전' 허울 뿐인 아시아 금융허브의 꿈 [외국 금융사 脫코리아]](https://img.etoday.co.kr/crop/140/88/2100022.jpg)
![[단독]"한 번 뗄 때마다 수 백만원 수령 가능" 가짜 용종 보험사기 기승](https://img.etoday.co.kr/crop/140/88/2100020.jpg)
![8만 달러 터치한 비트코인, 연내 '10만 달러'도 넘보나 [Bit코인]](https://img.etoday.co.kr/crop/140/88/2100256.jpg)

![환자복도 없던 우즈베크에 ‘한국식 병원’ 우뚝…“사람 살리는 병원” [르포]](https://img.etoday.co.kr/crop/140/88/2099863.jpg)
![불 꺼진 복도 따라 ‘16인실’ 입원병동…우즈베크 부하라 시립병원 [가보니]](https://img.etoday.co.kr/crop/140/88/2099872.jpg)
![“과립·멸균 생산, 독보적 노하우”...‘단백질 1등’ 만든 일동후디스 춘천공장 [르포]](https://img.etoday.co.kr/crop/140/88/2099348.jpg)







![[바이오 단신] 알피바이오, 신개념 건기식 젤리 '이지츄' 상표출원 外](https://img.etoday.co.kr/crop/85/60/2061147.jpg)






![잠자던 내 카드 포인트, ‘어카운트인포’로 쉽게 조회하고 현금화까지 [경제한줌]](https://img.etoday.co.kr/crop/300/170/2100528.jpg)
![사상 첫 8만1000달러 넘어선 비트코인 [포토]](https://img.etoday.co.kr/crop/300/190/2100561.jpg)