디지털헬스와 소프트웨어 의료기기가 임상 증가율 1위
의료 AI ‘루닛‧뷰노’, 디지털 치료기기 ‘에임메드‧웰트’ 대표
최근 5년간 식품의약품안전처에서 임상 승인을 받은 의료기기가 2배 가까이 증가한 것으로 나타났다. 특히 디지털헬스‧소프트웨어 의료기기(SaMD)의 임상이 가장 많이 증가했고, 시장에 출시된 혁신의료기기 비율도 가장 높았다.
20일 한국보건산업진흥원이 최근 발간한 ‘제1차 의료기기산업 실태조사 및 2023년 시장 동향 분석’ 자료에 따르면 이같이 확인됐다.
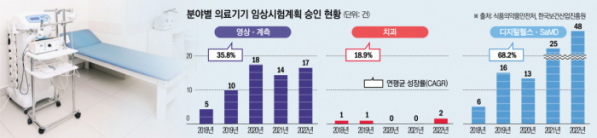
보고서에 따르면 2018년부터 2022년까지 식약처 승인을 받은 의료기기 임상시험은 총 620건이다. 2018년 88건에서 2022년 150건으로 늘었다. 이 기간 2021년을 제외하고 매년 승인 건수가 증가했다. 가장 많이 승인된 분야는 치료기기‧재료로 전체의 59%인 366건이 승인됐다.
증가율이 가장 높은 분야는 디지털헬스와 SaMD다. 2018년 임상시험 승인이 6건에 불과했지만, 2022년 48건으로 연평균 68.2% 증가하며 8대 분야(△영상‧계측 △체외진단 △치과 △고령화 △보건안보 △의료용로봇 △인체삽입형 △디지털헬스‧SaMD) 의료기기 중 임상시험계획 승인 증가율이 가장 높았다.
디지털헬스‧SaMD는 국내 의료기기 연구개발이 가장 활발하게 진행되고 있는 분야다. 의료 기술에 정보통신기술(ICT)을 결합한 산업으로 인공지능(AI) 의료기기와 디지털 치료기기 등이 대표적이다. 국내 의료AI 기업은 루닛, 뷰노 등을 필두로 국내와 해외에서 성과를 올리고 있으며, 디지털 치료기기는 에임메드와 웰트 등 4곳이 허가를 받았다.
이어 영상‧계측이 2018년 5건에서 2022년 17건 늘었고, 체외진단은 2018년 13건에서 코로나19가 발생한 2020년 53건으로 급증했으나, 2022년 6건으로 감소했다.
디지털헬스‧SaMD는 품목허가도 증가했다. 최근 5년간 신규 품목허가를 받은 제품은 총 320개로 이 기간 상승률은 36.4%에 달한다. 정부가 관련 규제와 제도를 마련하는 등 개발을 지원한 것이 이유다. 실제 정부는 디지털헬스 분야 육성을 위해 허가‧심사 및 임상시험계획서 작성을 위한 가이드라인을 마련하고 디지털 치료기기 등 관련 의료기기 개발을 적극 지원했다.
식약처의 최종 승인을 받은 혁신의료기기도 디지털헬스가 가장 많다. 식약처는 최근 3년(2021~2023) 48건의 제품을 혁신의료기기로 지정했으며, 이중 최종 승인을 받은 제품은 22건이다. 디지털헬스가 15건(68.2%)으로 가장 많고, 치료기기‧재료 분야 4건(18.2%), 체외진단 2건(9.1%), 영상계측 1건(4.5%) 순이다.
업계에서는 디지털헬스‧SaMD가 신산업이어서 관심도가 높아 발전하고 있다고 분석했다. 하지만 상승세를 이어가려면 기업은 시장에서 증명해야 하고, 중장기적인 정책도 필요하다고 입을 모은다.
의료 AI 업계 관계자는 “의료 AI에 한정해 말하면 시장에 이미 공급된 제품이 많아 승인 건수도 증가했다고 생각한다. 앞으로도 임상은 증가할 것으로 기대하고 있다”면서도 “흐름을 이어가기 위해서는 임상을 통해 가치를 입증하는 것이 중요하다”고 말했다.
디지털 의료기기 업계 관계자는 “기존에 없던, 새롭게 시작하는 산업이어서 관심이 높고 비전이 있다고 생각해 증가했다고 생각한다”며 “이제 기업은 시장에 대한 확신을 줘야 한다. 이 시장은 기업만 잘하는 것이 아니라 정부, 의료계 등 모두의 노력이 필요해 중장기적인 환경을 고려한 정책이나 설계 지원이 필요하다”고 조언했다.

![어떤 주담대 상품 금리가 가장 낮을까? ‘금융상품 한눈에’로 손쉽게 확인하자 [경제한줌]](https://img.etoday.co.kr/crop/140/88/2101515.jpg)
![2025 수능 시험장 입실 전 체크리스트 [그래픽 스토리]](https://img.etoday.co.kr/crop/140/88/2101156.jpg)
!["최강야구 그 노래가 애니 OST?"…'어메이징 디지털 서커스'를 아시나요? [이슈크래커]](https://img.etoday.co.kr/crop/140/88/2101671.jpg)


















![[찐코노미] 美 취약점을 파고든 K방산의 미래…차기 방산 대장주는 '이것'?](https://img.etoday.co.kr/crop/300/170/2101653.jpg)
![예결위, 비경제부처 예산심사 첫날 [포토]](https://img.etoday.co.kr/crop/300/190/2101714.jpg)