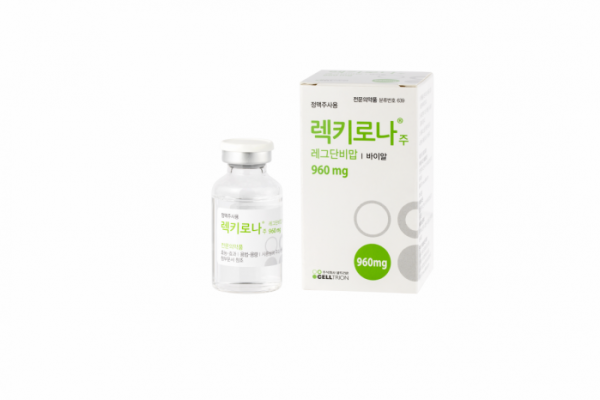
셀트리온의 코로나19 항체 치료제가 유럽 내 품목허가를 위한 절차를 밟는다.
셀트리온은 25일 유럽의약품청(EMA)이 코로나19 항체치료제 렉키로나(개발명:CT-P59, 성분명:레그단비맙)에 대한 롤링 리뷰(순차 심사)에 들어가 품목허가를 위한 공식 검토 절차를 시작했다고 밝혔다.
EMA의 롤링 리뷰는 EMA 산하 약물사용자문위원회(CHMP)에서 팬데믹 등 위기상황 시 유망한 치료제 또는 백신의 평가를 가속화하기 위해 활용하는 제도로, 최종 허가 신청 전 실시간으로 의약품의 유효성, 안전성, 품질 등에 대한 데이터와 문서 등을 회사에서 제출받고 이를 신속히 검토하는 방식이다.
셀트리온은 렉키로나의 신속한 글로벌 허가를 진행하기 위해 이미 품질 및 제조공정 관리, 비임상 시험, 임상시험 데이터를 EMA에 제출했고, CHMP는 셀트리온이 제출한 각종 데이터를 기반으로 렉키로나의 효능 및 안전성 등에 대한 평가를 시작한다.
셀트리온은 렉키로나의 글로벌 임상 2상 종료 후 유럽 EMA를 비롯해 미국 식품의약국(FDA) 등 세계 주요 국가 규제기관들과 신속 승인 절차를 진행하기 위한 사전 협의를 진행해 왔다.
셀트리온 관계자는 “올해 2월 초 렉키로나의 식약처 조건부 품목 허가를 획득한 이후 국내 의료기관에 렉키로나를 원활히 공급하고 있고, 이번 EMA의 롤링 리뷰 착수를 통해 유럽 공급을 위한 허가 절차도 본격화됐다”라며 “현재 세계 주요 국가들과도 사전 협의가 진행되고 있는 만큼 각국 규제기관이 요청하는 각종 데이터와 서류를 차질없이 제출해 글로벌 팬데믹 사태 종식을 위한 렉키로나 조기 공급을 위해 최선을 다하겠다”라고 말했다.

![잠자던 내 카드 포인트, ‘어카운트인포’로 쉽게 조회하고 현금화까지 [경제한줌]](https://img.etoday.co.kr/crop/140/88/2100528.jpg)
!['20년 째 공회전' 허울 뿐인 아시아 금융허브의 꿈 [외국 금융사 脫코리아]](https://img.etoday.co.kr/crop/140/88/2100022.jpg)
![[단독]"한 번 뗄 때마다 수 백만원 수령 가능" 가짜 용종 보험사기 기승](https://img.etoday.co.kr/crop/140/88/2100020.jpg)
![8만 달러 터치한 비트코인, 연내 '10만 달러'도 넘보나 [Bit코인]](https://img.etoday.co.kr/crop/140/88/2100256.jpg)

![환자복도 없던 우즈베크에 ‘한국식 병원’ 우뚝…“사람 살리는 병원” [르포]](https://img.etoday.co.kr/crop/140/88/2099863.jpg)
![불 꺼진 복도 따라 ‘16인실’ 입원병동…우즈베크 부하라 시립병원 [가보니]](https://img.etoday.co.kr/crop/140/88/2099872.jpg)
![“과립·멸균 생산, 독보적 노하우”...‘단백질 1등’ 만든 일동후디스 춘천공장 [르포]](https://img.etoday.co.kr/crop/140/88/2099348.jpg)













![잠자던 내 카드 포인트, ‘어카운트인포’로 쉽게 조회하고 현금화까지 [경제한줌]](https://img.etoday.co.kr/crop/300/170/2100528.jpg)
![코스피 1% 이상 하락... 2531.66에 마감 [포토]](https://img.etoday.co.kr/crop/300/190/2100641.jpg)