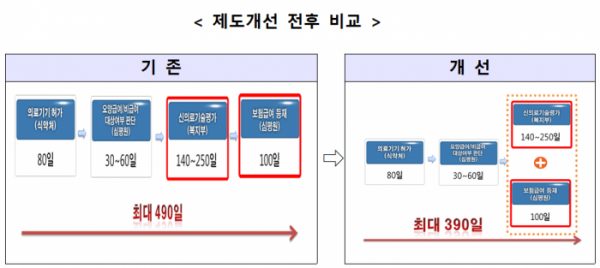
앞으로 신의료기술평가 시 국민건강보험급여 등재 심사가 동시 진행된다. 신개발 의료기기가 시장에 진입하는 기간이 100일가량 단축될 것으로 기대된다.
보건복지부는 이 같은 내용의 ‘신의료기술평가에 관한 규칙’ 개정안을 9일부터 다음 달 16일까지 입법예고한다고 7일 밝혔다. 이번 규칙 개정은 지난해 7월 발표된 ‘의료기기 규제혁신 및 산업 육성방안’의 후속조치다. 기존에는 신의료기술평가(140~250일)가 끝난 뒤 보험급여 등재 심사(100일)가 진행돼 신개발 의료기기의 시장 진입까지 최대 490일이 걸렸다.
이에 한국보건의료연구원과 건강보험심사평가원은 지난해 8월부터 12월까지 협의체를 구성해 구체적인 방안을 모색했다. 그 결과 신의료기술평가 시 보건의료연구원에 보험급여 등재를 위한 비용효과 자료 등을 제출하는 경우, 보험 등재 심사도 자동으로 진행하기로 했다. 개정 규칙이 시행되면 신개발 의료기기의 시장 진입 기간은 최대 390일로 100일가량 단축된다.
손호준 복지부 의료자원정책과장은 “신개발 의료기기의 시장 진입 기간이 100일가량 단축됨에 따라 그간 시장 진입 기간이 길어져 발생했던 업계의 어려움이 상당 부분 해소될 것”이라고 기대했다. 복지부는 입법예고 기간 중 국민 의견을 폭넓게 수렴한 후 개정안을 확정할 예정이다. 개정안에 의견이 있는 단체나 개인은 복지부 의료자원정책과에 문의하면 된다.

![긁어 부스럼 만든 발언?…‘티아라 왕따설’ 다시 뜨거워진 이유 [해시태그]](https://img.etoday.co.kr/crop/140/88/2100644.jpg)
![잠자던 내 카드 포인트, ‘어카운트인포’로 쉽게 조회하고 현금화까지 [경제한줌]](https://img.etoday.co.kr/crop/140/88/2100528.jpg)
![[단독]"한 번 뗄 때마다 수 백만원 수령 가능" 가짜 용종 보험사기 기승](https://img.etoday.co.kr/crop/140/88/2100020.jpg)
![8만 달러 터치한 비트코인, 연내 '10만 달러'도 넘보나 [Bit코인]](https://img.etoday.co.kr/crop/140/88/2100256.jpg)

![환자복도 없던 우즈베크에 ‘한국식 병원’ 우뚝…“사람 살리는 병원” [르포]](https://img.etoday.co.kr/crop/140/88/2099863.jpg)





!["한국은 '이것' 가능한 유일무이한 국가" 방산주 '이렇게' 투자할 때입니다 ㅣ 이영훈 이사 [찐코노미]](https://i.ytimg.com/vi/B9X9jpK5FGE/mqdefault.jpg)

![다시 ‘트럼프 시대’, 국회는?…무역장벽·리쇼어링 대비 [관심法]](https://img.etoday.co.kr/crop/85/60/2100699.jpg)
![부정평가 커진 尹...후반기 '양극화 타개' 주력[종합]](https://img.etoday.co.kr/crop/85/60/2098947.jpg)




![尹 "임기 후반 소득·교육 불균형 등 양극화 타개 노력"[종합]](https://img.etoday.co.kr/crop/85/60/2099177.jpg)


![[찐코노미] "한국은 이것 가능한 유일무이한 국가"…방산주 '이렇게' 투자할 때](https://img.etoday.co.kr/crop/300/170/2100715.jpg)
![코스피 1% 이상 하락... 2531.66에 마감 [포토]](https://img.etoday.co.kr/crop/300/190/2100641.jpg)