화이자와 독일 제약벤처 바이오엔테크가 공동 개발 중인 코로나19 백신 2종이 13일(현지시간) 미국 식품의약국(FDA)의 ‘패스트트랙(Fast Track)’에 지정됐다고 홍콩 영자지 사우스차이나모닝포스트(SCMP)가 보도했다.
코로나19 백신이 FDA의 패스트트랙에 지정된 것은 지난 5월 모더나에 이어 두 번째다.
화이자와 바이오엔테크는 RNA 백신 후보 4종에 대해 임상시험을 진행하고 있는데 그중 개발이 가장 진전된 2종이 FDA의 우선 심사 대상인 패스트트랙에 올랐다. 해당 백신 후보 물질은 ‘BNT162b1’과 ‘BNT162b2’다. 이달 중 시작할 예정인 대규모 임상시험 결과가 좋으면 FDA가 승인 절차를 우선적으로 진행, 신속한 출시로 이어질 수 있다.
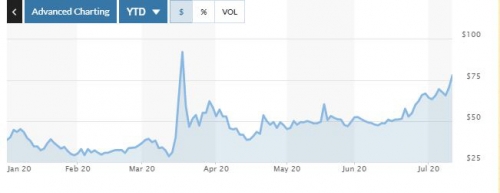
이 소식에 화이자 주가는 이날 4.1% 급등한 35.21달러로 마감했다. 바이오엔테크 미국주식예탁증서(ADR)는 10.6% 폭등했다. 바이오엔테크 ADR는 나스닥거래소에서 올 들어 지금까지 약 130% 뛰었다. 그만큼 코로나19 백신에 대한 기대가 크다는 증거다.
화이자와 바이오엔테크 모두 코로나19 백신 개발에 강한 자신감을 보이고 있다. 양사는 지난 1일 백신 후보 물질 중 하나인 ‘BNT162b1’ 초기 임상시험 결과를 공개하면서 접종자들이 바이러스를 무력화할 수 있는 중화항체를 형성했다고 밝혔다.
앨버트 불라 화이자 회장 겸 최고경영자(CEO)는 이달 초 미국 잡지 타임과의 인터뷰에서 “임상시험 결과에 따라 이르면 10월에도 백신 공급을 개시할 수 있다”며 “우리는 승인 취득 전부터 생산을 시작하는 이례적인 결정을 내렸다. 실용화에 실패하면 개발에 들어간 10억~20억 달러(약 1조2000억~2조4000억 원) 비용은 손실로 계상할 뿐”이라고 말했다.
위구르 사한 바이오엔테크 CEO는 지난 10일 월스트리트저널(WSJ)과의 인터뷰에서 “연말까지 당국에 백신 승인 신청을 할 준비가 될 것”이라며 “내년 말에는 생산량이 10억 개 이상에 이를 수 있다”고 낙관론을 펼쳐 뉴욕증시 상승을 이끌기도 했다.

!['20년 째 공회전' 허울 뿐인 아시아 금융허브의 꿈 [외국 금융사 脫코리아]](https://img.etoday.co.kr/crop/140/88/2100022.jpg)
![[단독]"한 번 뗄 때마다 수 백만원 수령 가능" 가짜 용종 보험사기 기승](https://img.etoday.co.kr/crop/140/88/2100020.jpg)
![8만 달러 터치한 비트코인, 연내 '10만 달러'도 넘보나 [Bit코인]](https://img.etoday.co.kr/crop/140/88/2100256.jpg)

![환자복도 없던 우즈베크에 ‘한국식 병원’ 우뚝…“사람 살리는 병원” [르포]](https://img.etoday.co.kr/crop/140/88/2099863.jpg)













![[뉴욕인사이트] ‘트럼프 랠리’ 이어갈까…소비자물가 주목](https://img.etoday.co.kr/crop/85/60/2098764.jpg)


![[정치대학]이재명, 정치운명 가를 ‘운명의 주’…시나리오별 파장은?](https://img.etoday.co.kr/crop/300/170/2100294.jpg)
![사상 첫 8만1000달러 넘어선 비트코인 [포토]](https://img.etoday.co.kr/crop/300/190/2100561.jpg)