올해 하반기부터 저투자·저품질 복제약(제네릭) 값이 내린다.
보건복지부는 27일 제네릭 의약품의 가격 제도를 동일제제-동일가격 원칙에서 개발 노력에 따른 차등가격 원칙으로 개편하는 내용의 ‘제네릭 의약품 약가제도 개편방안’을 발표했다.
이번 개편방안은 지난해 발사르탄(고혈압약 원료) 원료의약품 2개 품목에서 발암물질인 N-니트로소디메틸아민이 검출된 것을 계기로 제네릭 제도 전반에 대한 개편이 필요하다는 판단에 따라 마련됐다. 당시 발사르탄 사태는 공동 생물학적 동등성 시험 제도와 높은 제네릭 약가 수준으로 인한 제네릭의 난립 및 원료 품질관리 미비가 주요 원인으로 지적됐다.
이에 복지부는 식품의약품안전처와 실무협의체를 구성·운영해 허가부터 약가 제도까지 제네릭 제도 전반을 검토하고 개편 방향을 논의했다.
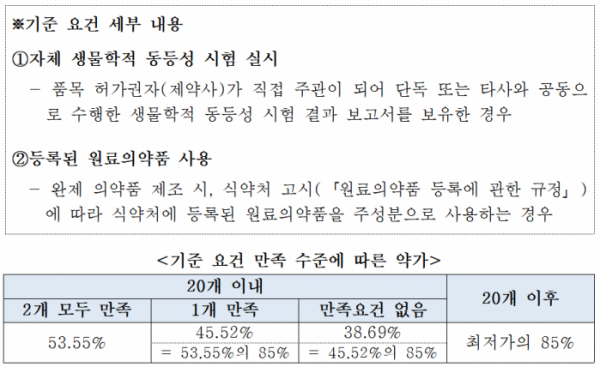
그 결과 정부는 자체 생물학적 동등성 시험 실시 여부와 등록된 원료의약품 사용 여부에 따라 제네릭 의약품 가격을 산정하기로 했다. 우선 제네릭 등재순번 20번째까지 제품군에 대해선 두 요건을 모두 충족하는 경우 원조 의약품 가격의 53.55%를 적용한다. 한 요건만 만족하면 45.52%, 만족 요건이 없을 경우에는 38.69%로 약가를 산정한다.
등재순번 20번째 이후부턴 앞 순번 제네릭 의약품 중 최저가의 85%를 적용한다.
복지부 관계자는 “제약사의 책임성을 강화시키고, 개발을 위한 시간과 비용 투자 등의 노력 여부에 따라 보상체계가 다르게 적용되도록 했다”며 “특히 그간 제약업계에서 우려를 나타낸 일괄적인 약가 인하 방식이 아닌 차등 가격 체계 운영을 통해 제약사에서 신약 개발 동력을 계속 확보할 수 있도록 했다”고 설명했다.
이번 개편방안은 ‘약제의 결정 및 조정기준(복지부 고시)’ 개정을 거쳐 이르면 올해 하반기부터 시행된다. 단 복지부는 제약계 및 의료 현장의 혼란 최소화를 위해 신규 제네릭과 기존에 등재된 제네릭(건강보험 급여 적용 중인 제네릭)으로 구분해 적용 시점을 달리할 계획이다.

![어떤 주담대 상품 금리가 가장 낮을까? ‘금융상품 한눈에’로 손쉽게 확인하자 [경제한줌]](https://img.etoday.co.kr/crop/140/88/2101515.jpg)
![2025 수능 시험장 입실 전 체크리스트 [그래픽 스토리]](https://img.etoday.co.kr/crop/140/88/2101156.jpg)
!["최강야구 그 노래가 애니 OST?"…'어메이징 디지털 서커스'를 아시나요? [이슈크래커]](https://img.etoday.co.kr/crop/140/88/2101671.jpg)



















![[찐코노미] 美 취약점을 파고든 K방산의 미래…차기 방산 대장주는 '이것'?](https://img.etoday.co.kr/crop/300/170/2101653.jpg)
![예결위, 비경제부처 예산심사 첫날 [포토]](https://img.etoday.co.kr/crop/300/190/2101714.jpg)