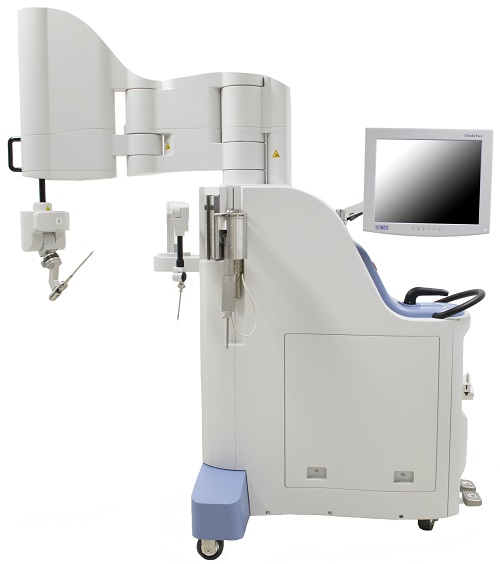
큐렉소(060280)는 19일 자회사인 씨티씨(CTC, Curexo Technology Corporation / 미국 프리먼트 소재)가 인공관절 수술로봇 로보닥 신규버전(V2.0)의 고관절치환술(THA)에 대한 FDA 승인을 완료했다고 밝혔다.
이번 FDA 승인을 받은 로보닥 V2.0은 현재 사용 중인 로보닥을 보완한 업그레이드 제품으로 획기적이라는 평가를 받고 있다. 2012년 하반기 연구개발에 착수 했으며, 지난 3월 11일 FDA 승인 신청을 낸 후 완료까지 약 5개월이 소요된 것으로 나타났다.
먼저, 기존 로보닥 시스템은 수술을 계획하는 워크스테이션인 올소닥(Orthodoc)과 수술로봇 베이스, 그리고 로봇 콘트롤 캐비닛으로 구성되어 있었지만, 신제품은 수술 계획 워크스테이션은 유저인터페이스와 기능이 개선된 티플랜(T-Plan)으로 변경 되었고, 수술로봇은 로봇의 베이스 안에 로봇 콘트롤러가 통합된 티캣(T-CAT, Computer Assisted Tool)으로 변경되어 수술실 내의 공간활용도와 사용자 편의성을 증대시켰다.
티캣(T-CAT)의 운영시스템도 기존의 DOS에서 리눅스 기반의 큐엔엑스(QNX)로 변경되었으며, 통신 시스템과 하드웨어 구성품을 업그레이드하여 데이터 처리 및 하드웨어 지원속도를 빠르고 안정적으로 개선시켜 향후 더욱 다양한 수술기법 응용이 가능해 질 전망이다.
뿐만 아니라, 핵심부품인 매니퓰레이터(Manipulator, 로봇암)도 기존 산교社 제품에서 자체 설계, 제작품으로 변경되어 수급 및 유지보수에 신속한 대응이 가능해졌다.
큐렉소 이재준 대표는 “더 나은 수술결과를 위한 사려 깊은 솔루션을 제공한다는 의미를 담은 씨티씨의 뉴 비즈니스 브랜드 ‘씽크서지칼(THINK Surgical)’을 기반으로 티플랜(T-Plan)과 티캣(T-CAT)이 탄생되었다”며 “이는 미국과 유럽을 중심으로 한 본격적인 수술로봇 의료기 시장 진출의 비전을 담은 것으로 2015년부터 미국 판매를 시작으로 전 세계 판매를 이어 갈 것” 이라고 말했다.
또한, 슬관절치환술(TKA) 부분의 FDA 승인 신청을 위한 계획도 차질 없이 준비 중 이라며, 슬관절 부분의 로보닥 수술 경험이 많은 한국과 독일의 의료진과 협력하는 등 최상의 결과를 끌어내기 위해 노력하고 있다고 전했다.

!['20년 째 공회전' 허울 뿐인 아시아 금융허브의 꿈 [외국 금융사 脫코리아]](https://img.etoday.co.kr/crop/140/88/2100022.jpg)
![[단독]"한 번 뗄 때마다 수 백만원 수령 가능" 가짜 용종 보험사기 기승](https://img.etoday.co.kr/crop/140/88/2100020.jpg)
![8만 달러 터치한 비트코인, 연내 '10만 달러'도 넘보나 [Bit코인]](https://img.etoday.co.kr/crop/140/88/2100256.jpg)

![환자복도 없던 우즈베크에 ‘한국식 병원’ 우뚝…“사람 살리는 병원” [르포]](https://img.etoday.co.kr/crop/140/88/2099863.jpg)






![불 꺼진 복도 따라 ‘16인실’ 입원병동…우즈베크 부하라 시립병원 [가보니]](https://img.etoday.co.kr/crop/85/60/2099872.jpg)
![[BioS]한미약품, 11일 기관투자자 대상 기업설명회 열어](https://img.etoday.co.kr/crop/85/60/2100453.jpg)






![“과립·멸균 생산, 독보적 노하우”...‘단백질 1등’ 만든 일동후디스 춘천공장 [르포]](https://img.etoday.co.kr/crop/85/60/2099348.jpg)
![[정치대학]이재명, 정치운명 가를 ‘운명의 주’…시나리오별 파장은?](https://img.etoday.co.kr/crop/300/170/2100294.jpg)
![한경협 ‘미국 신정부 출범, 한국 경제 준비되었는가’ 좌담회 [포토]](https://img.etoday.co.kr/crop/300/190/2100445.jpg)