인태반 주사제 6개 제품 중 5개가 시장에서 퇴출됐다. 식품의약품안전청은 전체 인태반 유래 의약품에 대한 임상재평가 계획에 따라 '자하거(태반) 가수분해물 주사제' 6개 업체 6개 품목에 대하여 재평가 결과를 14일 공시했다.
가수분해물이란 하나의 분자 또는 이온이 물의 개입에 의해서 두개의 분자 또는 이온으로 분해되어 생성된 산물이다.
식약청은 이번 '자하거 가수분해물 주사제'의 재평가 결과 GCJBP의 '지씨제이비피라이넥주'는 유용성이 인정돼 지난해 12월 최종 공시했다. 나머지 5개 품목의 경우 자료를 미제출한 드림파마의 '클라틴주' 등 2품목에 대해서는 지난 11일 허가취소했고 경남제약 '플라젠주' 등 3개 품목은 유용성을 불인정했다고 발표했다.
유용성 불인정 품목은 행정처분(허가 취소 및 시중 유통품에 대한 회수ㆍ폐기 등) 관련 절차를 밝을 예정이며 관련 협회 등을 통해 동 제품이 처방되는 일이 없도록 했다. 이 대상은 경남제약 '플라젠주'와 광동제약 '휴로센주', 대원제약 '뉴트론주'이다.
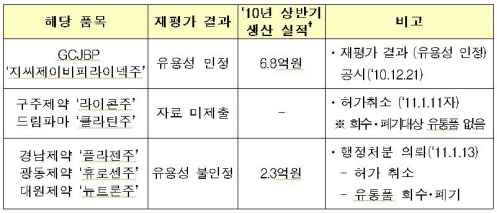
경남제약은 이 결과에 대해 불만을 표시했지만 나머지 두 업체들은 받아들였다. 광동제약 관계자는 "식약청이 결정한 사항이기 때문에 결과를 받아들이겠다"고 말했다. 대원제약 관계자는 "'뉴트론주'는 현재 시중에 판매되고 있지 않기 때문에 식약청의 평가 결과에 대해 신경쓸 문제가 아닌 것 같다"고 얘기했다.
반면 녹십자와 일본제약업체의 합자회사인 지씨제이비피(GCJBP)의 태반주사인 지씨제이비피라이넥주는 유용성을 인정받아 허가가 유지됐다.
식약청은 지난 2006년 인태반 유래 의약품에 대해 국내 임상시험을 통해 안전성ㆍ유효성을 재검증하기로 결정하고 자하거 추출물 주사제와 가수분해물 주사제, 자하거엑스 함유 복합액제의 임상재평가를 단계적으로 실시했다.

!['20년 째 공회전' 허울 뿐인 아시아 금융허브의 꿈 [외국 금융사 脫코리아]](https://img.etoday.co.kr/crop/140/88/2100022.jpg)
![[단독]"한 번 뗄 때마다 수 백만원 수령 가능" 가짜 용종 보험사기 기승](https://img.etoday.co.kr/crop/140/88/2100020.jpg)
![8만 달러 터치한 비트코인, 연내 '10만 달러'도 넘보나 [Bit코인]](https://img.etoday.co.kr/crop/140/88/2100256.jpg)

![환자복도 없던 우즈베크에 ‘한국식 병원’ 우뚝…“사람 살리는 병원” [르포]](https://img.etoday.co.kr/crop/140/88/2099863.jpg)
















![[정치대학]이재명, 정치운명 가를 ‘운명의 주’…시나리오별 파장은?](https://img.etoday.co.kr/crop/300/170/2100294.jpg)
![이재명 민주당 대표, 손경식 경총회장 만나 [포토]](https://img.etoday.co.kr/crop/300/190/2100510.jpg)