올해 노벨 생리의학상은 일본 도쿄공업대 명예교수인 오스미 요시노리에게 돌아갔다. 이로써 일본은 3년 연속 과학분야 노벨상 수상이라는 기쁨을 맛봤다. 오스미 교수와 일본에게 노벨 생리의학상을 가져다 준 것은 자가포식 (Autophagy) 연구다. 자가포식은 세포내 단백질 재활용하는 면역 현상으로 암 노화 등 다양한 질병을 치료할 잠재력을 갖고 있다.
자가포식 (Autophagy)란?
우리 몸을 구성하는 세포는 대사물질을 이용해 에너지를 발생시키는 미토콘드리아(Mitochondria)와 단백질 합성에 관여하는 리보솜(Ribosome), 물질을 분해하는 효소를 가진 라이소좀(Lysosome) 등 다양한 세포 소기관(Organelle)을 가지고 있다.
세포 내에서 대사와 합성을 통해 만들어진 물질이 쓰임을 다하거나 산화 스트레스와 같은 요인으로 인해 내부 기관이 손상을 받았을 때 라이소좀에서 이를 분해하는 역할을 수행하는데 이 과정을 자가포식(Autophagy)이라고 한다.
1970년대 라이소좀의 발견 이후, 연구자들은 세포 내에는 큰 물질을 라이소좀까지 이동시키는 기전에 대한 연구를 진행해왔다. 오스미 교수는 스트레스 상황에서 평상시의 세포에서는 존재하지 않는 자가소포체(Autophagosome)가 생겨나 라이소좀까지 물질을 이동시킨다는 것을 현미경을 통해 관찰했다.
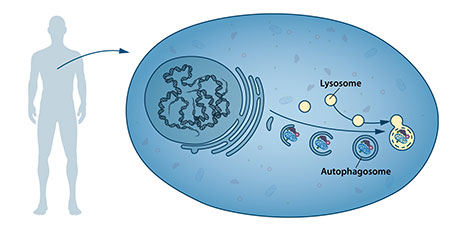
오스미 교수와 그 연구진들은 이후 다양한 유전자의 변형 실험을 통해 1992년, 자가소포체가 발생하는데 중요한 유전자를 최초로 발견했고 일련의 실험을 통해 자가포식의 메커니즘을 규명했다.
다양한 질환에 적용이 가능
자가포식은 세포의 생명유지와 리빌딩(re-building)에 필요한 에너지를 빠르게 제공해주고, 이는 외부의 스트레스에 대한 세포의 대응에 필수적이다. 세포가 자가포식을 이용해 손상된 단백질과 세포 소기관을 제거하고 건강한 상태를 유지함으로써 노화 작용에 대응하는 데 중요한 역할을 할 것으로 기대된다.
또한 뇌세포에서의 베타-아밀로이드(Aβ) 축적이 원인으로 알려져 있는 알츠하이머, 도파민 세포의 파괴로 발생하는 파킨슨 병과 같은 뇌질환도 자가포식의 교란에 의한 것이 밝혀졌다. 이를 바탕으로 다양한 질병에서 자가포식을 타깃으로 하는 약물 개발이 이뤄지고 있다.
백찬기 서울아산병원 융합의학과 교수는 “자가포식 작용은 최근 암, 근육 기능 이상 질환, 퇴행성 신경질환, 감염질환, 노화 등 다양한 질병에 관여되고 있는 것으로 밝혀지고 있다”면서 “국내에서도 자가포식 연구에 좀 더 집중하면 부작용을 최소화할 수 있는 항암제와 신경질환 치료제 등을 개발할 수 있을 것”이라고 말했다.
꾸준한 기초 연구에 대한 투자가 이뤄낸 업적
일본은 오스미 교수를 포함해서 22명의 과학 분야의 노벨상 수상자를 배출했다. 이러한 수상 배경에는 정부와 기업의 꾸준한 기초 연구에 대한 투자가 큰 요인으로 작용했다.
일본의 경우, 기업들의 기초과학분야 투자가 활발해 2014년 일본 과학기술 연구비 18조9700억엔의 70%를 웃도는 13조5800억엔의 투자가 이뤄졌다. 또한 정권의 교체에도 흔들리지 않는 지속적인 지원으로 인해 연구자들의 안정적인 연구 환경이 조성된 것도 큰 이점으로 뽑힌다.
현장의 연구자들은 노벨상을 원하는 사회 분위기와는 다르게 지속적인 투자가 이뤄지지 않는 점에 대해 불만을 나타냈다. 반짝 인기 몰이하는 이슈에만 자원이 쏠리다 보니 일본처럼 장기간 한 가지를 연구하는 것이 어려운 실정이다.
한 의대교수는 "노벨생리의학상은 글로벌에서 우리의 자연과학의 수준을 나타내는 것으로 개인이 탁월하다고 받을 수 있는 것도 아니며 일회성 수상은 큰 의미가 없다"면서 "당장의 성과에만 매달리기 보다는 긴 인내심을 가지고 장기적인 투자를 하는 것이 우리나라 기초 과학 분야 연구에 자양분이 될 것"이라고 강조했다.

![어떤 주담대 상품 금리가 가장 낮을까? ‘금융상품 한눈에’로 손쉽게 확인하자 [경제한줌]](https://img.etoday.co.kr/crop/140/88/2101515.jpg)
![2025 수능 시험장 입실 전 체크리스트 [그래픽 스토리]](https://img.etoday.co.kr/crop/140/88/2101156.jpg)
!["최강야구 그 노래가 애니 OST?"…'어메이징 디지털 서커스'를 아시나요? [이슈크래커]](https://img.etoday.co.kr/crop/140/88/2101671.jpg)


















![[찐코노미] 美 취약점을 파고든 K방산의 미래…차기 방산 대장주는 '이것'?](https://img.etoday.co.kr/crop/300/170/2101653.jpg)
![예결위, 비경제부처 예산심사 첫날 [포토]](https://img.etoday.co.kr/crop/300/190/2101714.jpg)