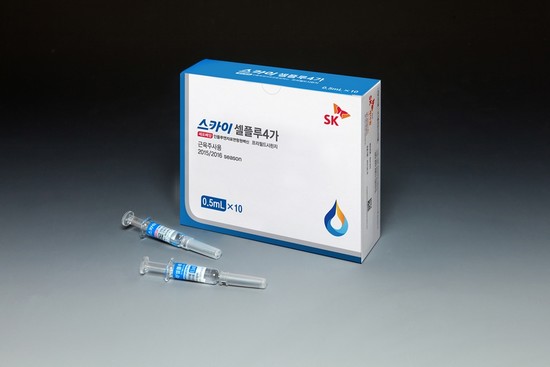
SK케미칼은 ‘스카이셀플루’가 만 3세~18세 소아·청소년용으로 식품의약안전처의 시판 허가를 획득했다고 2일 밝혔다.
스카이셀플루는 세포배양 방식의 4가 독감백신으로 SK케미칼이 세계 최초로 개발, 지난해 12월 성인용 허가를 획득했고 이번에 소아·청소년용까지 접종 범위를 확대했다. 이에 올가을부터 만 3세 이상 전 연령층을 대상으로 첫 접종에 들어가게 됐다.
스카이셀플루 4가는 한 번의 접종으로 네 종류 독감 바이러스를 예방할 수 있는 차세대 백신이다. 스카이셀플루 4가 백신은 A형 독감 바이러스 두 종류(H1N1, H3N2)와 B형 바이러스 두 종류(야마가타, 빅토리아)를 모두 예방할 수 있다. 기존 3가 백신을 맞고도 B형 독감에 걸리는 사례가 많아지면서 2012년부터 세계보건기구(WHO), 유럽의약품청(EMA)도 4가 백신 접종을 권장하고 있다.
또 스카이셀플루는 세포배양 백신으로 계란에서 백신을 생산하던 기존 방식과 달리 무균 배양기를 통해 생산돼 항생제나 보존제가 필요 없는 것이 특징이다. 계란 알레르기에 대한 부담이 없고 생산 기간도 기존 백신보다 절반 가까이 줄어 독감 대유행 시 가장 빠른 대응이 가능한 것이 최대 장점이다.
SK케미칼 박만훈 사장은 “차세대 백신을 통해 소아에서 성인까지 모든 세대에서 독감 예방 효과를 볼 수 있을 것”이라며 “앞으로도 다양한 프리미엄 백신 개발을 통해 국가 백신주권 확립에 기여할 것”이라고 말했다.
한편 SK케미칼은 2008년부터 백신 연구 개발에 착수, 인프라 구축과 R&D에 약 4000억원의 투자를 진행해왔고 식약처, 보건복지부, 산자부, 경상북도, 안동시 등 정부 부처 및 지자체와의 적극적인 협력을 통해 4가 세포배양 독감백신 상용화라는 성과를 거뒀다. 지난달 27일엔 SK케미칼이 개발한 혈우병 치료제 ‘NBP601’이 국내 바이오 신약으로는 최초로 미국 FDA의 시판 허가를 획득, 바이오 신약의 새 역사를 쓰기도 했다.

![어떤 주담대 상품 금리가 가장 낮을까? ‘금융상품 한눈에’로 손쉽게 확인하자 [경제한줌]](https://img.etoday.co.kr/crop/140/88/2101515.jpg)
![2025 수능 시험장 입실 전 체크리스트 [그래픽 스토리]](https://img.etoday.co.kr/crop/140/88/2101156.jpg)
!["최강야구 그 노래가 애니 OST?"…'어메이징 디지털 서커스'를 아시나요? [이슈크래커]](https://img.etoday.co.kr/crop/140/88/2101671.jpg)


















![[찐코노미] 美 취약점을 파고든 K방산의 미래…차기 방산 대장주는 '이것'?](https://img.etoday.co.kr/crop/300/170/2101653.jpg)
![예결위, 비경제부처 예산심사 첫날 [포토]](https://img.etoday.co.kr/crop/300/190/2101714.jpg)