
삼성바이오에피스는 유럽 종양학회 정기 학술대회(ESMO Virtual Congress 2020) 가상 전시회에서 ‘아바스틴’ 바이오시밀러 ‘에이빈시오’(성분명 베바시주맙)의 새로운 연구 결과를 공개한다고 15일 밝혔다.
지난해 같은 행사에서 에이빈시오의 글로벌 임상3상 결과를 발표한 발표했던 삼성바이오에피스는 추가 분석을 실시해 오리지널 의약품과의 임상의학적 동등성을 재차 입증할 수 있는 유의미한 데이터를 수집했다.
삼성바이오에피스는 임상 3상에 참여했던 비소세포폐암 환자 중 임상시험 프로토콜을 준수한 ‘순응 집단’으로 분류된 665명을 대상으로 에이빈시오와 오리지널 의약품 간 추가적인 비교 분석을 실시했다.
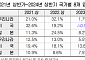
우선, 24주간의 ‘최고 전체반응률’에서 유의미한 치료 경과를 확인할 수 있는 11주 및 17주차의 데이터를 분석했다. 그 결과, 11주 및 17주차에 보인에이빈시오와 오리지널 의약품 간 최고 전체반응률 위험도 차이는 각각 2.2%(95% CI:-4.6%, 9.1%) 와 2.4%(95% CI: -5.1%, 10.0%)였고, 두 의약품간 유의미한 차이점이 발생하지 않았다.
두 번째로는 기준점 대비 종양 크기의 ‘최대 변화율’을 측정했다. 이는 치료 시작 시점을 기준으로 각 주차별로 종양이 가장 크게 감소한 비율의 평균값을 구한 것으로서, 이 결과 역시 에이빈시오와 오리지널 의약품 간 유의미한 차이점이 발생하지 않았다.
삼성바이오에피스가 진행한 에이빈시오 임상 3상 후속 연구결과의 자세한 내용은 17일(현지시간) e-포스터 형식으로 주최 측 디지털 플랫폼을 통해 공개될 예정이다.
삼성바이오에피스 관계자는 “임상 시험의 후속 연구를 통해 에이빈시오와 오리지널 의약품 간 의학적 효능이 동등한 수준임을 다시 한 번 입증할 수 있게 됐다”고 말했다.
에이빈시오는 지난 8월 유럽연합 집행위원회(EC)의 판매 허가를 획득한 국내 최초 아바스틴 바이오시밀러 제품이다. 삼성바이오에피스는 마케팅 파트너사 MSD(미국 Merck)와 함께 유럽 주요 5개국을 중심으로 ‘에이빈시오’의 본격적인 판매 체제에 돌입했다.

![[알림] 이투데이, '2024 CSR 영상공모전'... 27일까지 접수](https://img.etoday.co.kr/crop/140/88/2076324.jpg)
![‘어둠의 코시’ 프로야구 포스트시즌으로 향하는 매직넘버는? [해시태그]](https://img.etoday.co.kr/crop/140/88/2079369.jpg)

![Z세대의 말하기 문화, 사회적 유산일까 문제일까②[Z탐사대]](https://img.etoday.co.kr/crop/140/88/2079293.jpg)
![“AI·카메라 컨트롤 기능 기대감”…아이폰16 출시 첫날 ‘북적’ [르포]](https://img.etoday.co.kr/crop/140/88/2079108.jpg)





![[ENG/SUB]이제는 K팝 주류 버추얼 아이돌, 빌보드도 갈 수 있을까? #플레이브 #메이브 #나이비스 #이세계아이돌 [컬처콕플러스]](https://i.ytimg.com/vi/FBQW8Dy36Jw/mqdefault.jpg)









![[컬처콕 플러스] 플레이브가 쏜 버추얼 아이돌 붐…한계와 가능성은?](https://img.etoday.co.kr/crop/300/170/2079115.jpg)
![여성금융인 국제 콘퍼런스, 행사 요약하는 조경선 여성금융인네트워크 운영위원장 [포토]](https://img.etoday.co.kr/crop/300/190/2079429.jpg)