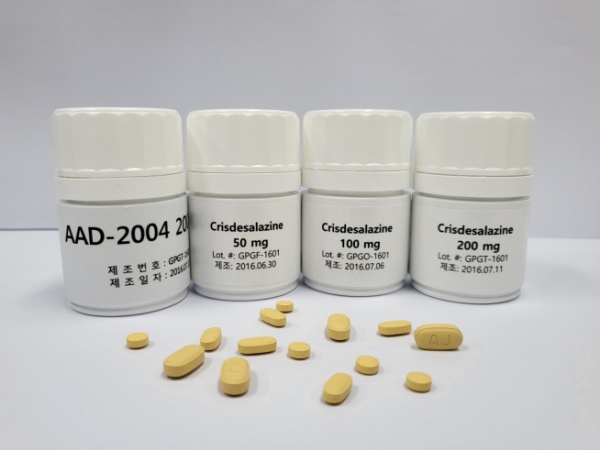
신약개발 벤처 지엔티파마는 알츠하이머와 치매 등 퇴행성 뇌질환과 우울증 치료제로 개발하고 있는 ‘크리스데살라진’의 임상 1b상에서 노인을 포함한 건강한 성인 40명에 대한 투약을 완료했다고 28일 밝혔다.
지엔티파마는 과학기술정보통신부 ‘21세기 뇌프론티어 연구개발사업’ 지원으로 자사가 발굴한 크리스데살라진을 알츠하이머 치매 신약으로 개발 중이다. 크리스데살라진은 mPGES-1 억제제로 염증 매개 물질인 프로스타글란딘 E2의 생성을 억제하고, 강력한 자유 라디칼 포착 작용으로 유해 물질인 활성산소를 제거하도록 고안한 다중표적 합성신약이다.
염증과 산화스트레스는 알츠하이머 치매, 루게릭병, 우울증과 같은 뇌질환 환자에게서 증가하며 질환을 일으키고 악화시킨다고 알려져 있다. 회사 측에 따르면 크리스데살라진은 비임상 연구에서 알츠하이머 치매의 3대 바이오마커(△아밀로이드 플라크 △타우병증 △신경세포 사멸)를 모두 줄이며 인지 기능을 향상하는 것으로 밝혀져 ‘네이처 뉴로사이언스’ 등 뇌신경 과학 분야 저명 학술지에 발표된 바 있다.
또한 인간의 알츠하이머 치매와 매우 유사하다고 알려진 반려견 인지기능장애증후군 임상 3상에서 확연한 약효와 안전성이 입증된 바 있다. 이에 따라 지난해 2월 농림축산검역본부로부터 국내 최초 동물용의약품 합성신약으로 승인받아 ‘제다큐어 츄어블정’이라는 상품명으로 출시됐다.
크리스데살라진은 건강한 성인 32명을 대상으로 완료한 임상 1a상 단회 상승용량시험에서 경구로 20~200mg을 투약했을 때 안전성이 검증된 바 있다.
지엔티마파는 이번에 등록 완료한 임상 1b상은 추가 단회 상승용량시험인 PART 2와 반복 상승용량시험인 PART 3로 구분해서 진행됐다. PART 2에서 600mg을 투여해도 중대 이상 반응이 나타나지 않았고, PART 3에서 200mg을 12시간 간격으로 15회 투여해도 건강한 성인은 물론 65세 이상 노인에게서도 안전성이 확인됐다고 회사 측은 설명했다. 크리스데살라진 100mg 경구 투여 후 생체 흡수율은 알츠하이머 치매 동물모델 및 반려견 인지기능장애증후군에서 최대 약효를 나타내는 크리스데살라진의 생체흡수율과 유사했다.
회사 측은 “건강한 성인 72명을 대상으로 진행한 임상 1상에서 크리스데살라진의 최대 목표 투여용량에서의 안전성이 확보됨에 따라 지엔티파마는 연내에 알츠하이머 치매 환자를 대상으로 한 임상 2상 시험계획서(IND)를 신청할 계획”이라고 설명했다.
이와 함께 지엔티파마 연구진은 루게릭병과 우울증 동물모델에서 크리스데살라진의 약효와 안전성을 입증해, 루게릭병과 우울증 환자에 대한 임상 2상도 진행할 예정이다.
곽병주 지엔티파마 대표이사는 “노인을 포함한 72명의 건강한 성인에게서 안전성이 확인됐고, 반려견 인지기능장애증후군 신약으로 승인받은 크리스데살라진이 알츠하이머 치매 치료제로 개발될 가능성이 매우 높다”며 크리스데살라진의 임상시험을 신속하고 효과적으로 진행해 신약으로 출시할 수 있도록 총력을 다할 것”이라고 강조했다.

![잠자던 내 카드 포인트, ‘어카운트인포’로 쉽게 조회하고 현금화까지 [경제한줌]](https://img.etoday.co.kr/crop/140/88/2100528.jpg)
!['20년 째 공회전' 허울 뿐인 아시아 금융허브의 꿈 [외국 금융사 脫코리아]](https://img.etoday.co.kr/crop/140/88/2100022.jpg)
![[단독]"한 번 뗄 때마다 수 백만원 수령 가능" 가짜 용종 보험사기 기승](https://img.etoday.co.kr/crop/140/88/2100020.jpg)
![8만 달러 터치한 비트코인, 연내 '10만 달러'도 넘보나 [Bit코인]](https://img.etoday.co.kr/crop/140/88/2100256.jpg)

![환자복도 없던 우즈베크에 ‘한국식 병원’ 우뚝…“사람 살리는 병원” [르포]](https://img.etoday.co.kr/crop/140/88/2099863.jpg)
![불 꺼진 복도 따라 ‘16인실’ 입원병동…우즈베크 부하라 시립병원 [가보니]](https://img.etoday.co.kr/crop/140/88/2099872.jpg)
![“과립·멸균 생산, 독보적 노하우”...‘단백질 1등’ 만든 일동후디스 춘천공장 [르포]](https://img.etoday.co.kr/crop/140/88/2099348.jpg)








![[바이오 단신] 알피바이오, 신개념 건기식 젤리 '이지츄' 상표출원 外](https://img.etoday.co.kr/crop/85/60/2061147.jpg)





![잠자던 내 카드 포인트, ‘어카운트인포’로 쉽게 조회하고 현금화까지 [경제한줌]](https://img.etoday.co.kr/crop/300/170/2100528.jpg)
![민주당, 국정농단 규탄·특검 촉구 천만인 서명운동본부 발대식 [포토]](https://img.etoday.co.kr/crop/300/190/2100572.jpg)