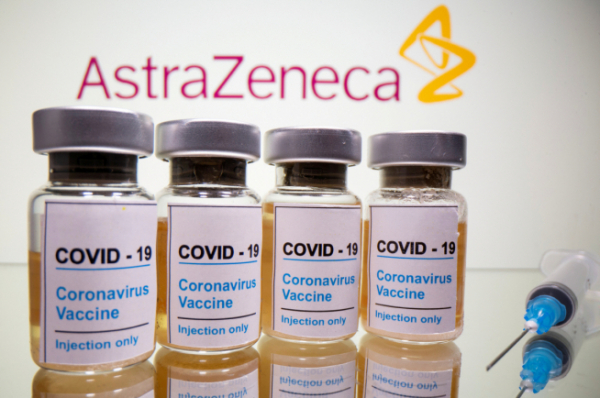
식품의약품안전처 검증자문단이 아스트라제네카 코로나19 백신의 고령자(만 65세 이상) 접종을 권고했다. 다만 검증자문단은 식약처의 3중 자문 중 첫 번째 검증 자문인 만큼 추후 이어질 △중앙약사심의위원회 △최종점검위원회 자문 결과에 따라 최종 허가 내용이 달라질 수 있다.
식약처 검증자문단은 한국아스트라제네카가 품목허가 신청한 ‘아스트라제네카 코비드-19백신주’을 만 65세 이상 고령자에도 사용할 것을 권고했다.
고령층에 대한 자료가 제한적이라는 한계에도 불구하고 애초 임상시험 계획이 만 18세 이상으로 설계됐고, 백신을 투여한 후 면역 반응이 성인(18∼64세)과 유사한 점, 중대한 이상 반응이 나타나지 않은 점 등을 중요하게 반영한 것이다.
백신의 예방효과를 분석하는 임상시험에 참여한 18세 이상의 성인 8895명 가운데 65세 이상 고령자 비율은 7.4%(660명), 2만3745명을 대상으로 한 안전성 평가에서 고령자는 8.9%(2109명) 정도에 그쳤다.
검증자문단은 고령층에 대한 자료가 제한적이지만, 임상시험이 만 18세 이상을 대상으로 유효성 및 안전성을 확인했고, 만 65세 이상을 포함한 전체 대상자에서 예방효과가 확인된 만큼 고령자 접종을 권고했다.
또 백신 투여 후 면역반응이 성인과 유사한 점도 판단에 반영됐다. 식약처는 아스트라제네카 코로나19 백신 접종 후 바이러스를 무력화하는 ‘중화항체’ 발생률이 성인(18~64세)과 고령자 사이에서 크게 차이나지 않았다고 밝혔다. 면역원성 평가에서 백신을 투여한 고령자에게 중화항체 생성비율은 64%, 성인은 80.7%로 나타났다.
박윤주 식약처 바이오생약심사부장은 “백신 접종 후 생성되는 결합항체나 중화항체는 면역력에 따라 달라질 수 있는데 고령자의 중화항체 양전율이 64%, 성인군의 중화항체 양전율이 80.7%라는 것은 60%가 넘었다는 측면에서 크게 차이가 없다고 판단했다”라고 말했다.
아스트라제네카 코로나19 백신을 둘러싼 고령층 접종 여부 논란은 계속해서 이어지고 있다. 유럽의약품청(EMA)에 이어 유럽연합(EU) 집행위원회에서는 29일(현지시간) 18세 이상을 대상으로 이 백신의 조건부 판매를 승인했다. 다만 임상 참여자가 대부분 18~55세라 55세가 넘는 연령대에서 얼마나 효과를 보일지는 아직 모른다고 판단했다.
독일의 질병관리청에 해당하는 로베르트코흐연구소(RKI) 산하 예방접종위원회는 28일(현지시간) 아스트라제네카 백신을 65세 미만에만 접종하라고 권고했다. 같은 날 에마뉘엘 마크롱 프랑스 대통령도 “아스트라제네카 백신은 65세 이상인 사람들에게 무효한 것과 다름없다고 본다”라며 “60∼65세 연령층에는 권유하지 않는다는 게 우리가 확보한 초기 결과”라고 언급했다. 이탈리아의약청(AIFA)도 30일(현지시간) 아스트라제네카 백신은 55세 이상에서 충분한 임상시험이 이뤄지지 않았다며 54세까지 성인에 우선 사용할 것을 권고했다.
김상봉 식약처 바이오생약국장은 “EU회원국에 따라 EMA 허가사항이 달라지는 게 허가 후 접종 과정에서 연령에 대한 권고가 있는 것으로 안다”라며 “이는 국가별 백신의 수급상황이 조금씩 다르다는 점도 고려된 것으로 보인다”라고 말했다.
식약처는 4일에 법정 자문기구인 ‘중앙약사심의위원회’에서 자문받고, 그 결과를 당일 공개할 예정이다. 김 국장은 “검증자문단 논의 결과를 중앙약사심의위원회에서 다시 논의해서 보다 입체적으로 점검한 뒤 최종 결론을 내도록 할 계획”이라고 말했다.

![잠자던 내 카드 포인트, ‘어카운트인포’로 쉽게 조회하고 현금화까지 [경제한줌]](https://img.etoday.co.kr/crop/140/88/2100528.jpg)
!['20년 째 공회전' 허울 뿐인 아시아 금융허브의 꿈 [외국 금융사 脫코리아]](https://img.etoday.co.kr/crop/140/88/2100022.jpg)
![[단독]"한 번 뗄 때마다 수 백만원 수령 가능" 가짜 용종 보험사기 기승](https://img.etoday.co.kr/crop/140/88/2100020.jpg)
![8만 달러 터치한 비트코인, 연내 '10만 달러'도 넘보나 [Bit코인]](https://img.etoday.co.kr/crop/140/88/2100256.jpg)

![환자복도 없던 우즈베크에 ‘한국식 병원’ 우뚝…“사람 살리는 병원” [르포]](https://img.etoday.co.kr/crop/140/88/2099863.jpg)
![불 꺼진 복도 따라 ‘16인실’ 입원병동…우즈베크 부하라 시립병원 [가보니]](https://img.etoday.co.kr/crop/140/88/2099872.jpg)
![“과립·멸균 생산, 독보적 노하우”...‘단백질 1등’ 만든 일동후디스 춘천공장 [르포]](https://img.etoday.co.kr/crop/140/88/2099348.jpg)













![잠자던 내 카드 포인트, ‘어카운트인포’로 쉽게 조회하고 현금화까지 [경제한줌]](https://img.etoday.co.kr/crop/300/170/2100528.jpg)
![코스피 1% 이상 하락... 2531.66에 마감 [포토]](https://img.etoday.co.kr/crop/300/190/2100641.jpg)