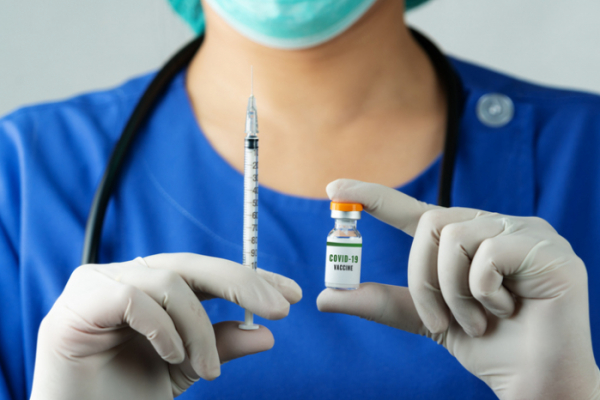
셀리드와 진원생명과학이 코로나19 백신 임상시험 1, 2상을 동시에 승인받았다.
식품의약품안전처는 국내 개발 코로나19 백신인 셀리드의 ‘AdCLD-CoV19’와 진원생명과학의 ‘GLS-5310’에 대한 임상시험을 4일 각각 승인했다. 이로써 현재 국내에서 코로나19 관련해 승인한 임상시험은 총 33건이고, 이 가운데 치료제 20건 백신 5건 총 25건이 임상시험 진행 중이다.
이번 임상시험은 건강한 성인을 대상으로 해당 백신의 안전성 및 면역원성을 평가하기 위한 1/2상 임상시험이다. 면역원성은 바이러스 감염성을 없애거나 낮추는 ‘중화항체’ 증가 비율이다. 해당 백신은 코로나19 바이러스의 ‘표면항원 유전자’를 아데노 바이러스 주형에 넣어 제조한 ‘바이러스벡터 백신’으로, 아데노 바이러스 주형을 통해 사람 세포 내로 전달된 표면항원 유전자가 체내에서 표면항원 단백질을 합성해 중화항체 생성을 유도하고, 이후 코로나19 바이러스가 침입했을 때 이 중화항체가 코로나19 바이러스를 제거하는 원리다.
영국 아스트라제네카, 중국 캔시노사, 러시아 가말레야연구소, 미국 존슨앤드존슨사 등 4개 다국적 제약사가 바이러스벡터 플랫폼의 코로나19 백신에 대한 3상 임상시험을 진행 중이다.
진원생명과학 역시 건강한 성인을 대상으로 백신의 안전성 및 면역원성을 평가하기 위한 1/2상 임상시험을 승인받았다. 진원생명과학의 백신은 코로나19 바이러스의 ‘표면항원 유전자’를 DNA(플라스미드) 형태로 제조한 ‘DNA 백신’이다. 접종한 코로나19 바이러스 표면항원 유전자에 의해 체내에서 표면항원 단백질을 합성해 중화항체 생성을 유도하고, 이후 코로나19 바이러스가 침입했을 때 이 중화항체가 코로나19 바이러스를 제거하게 되는 원리다.
DNA 백신은 국내의 제넥신, 미국 이노비오사가 현재 각각 1/2상, 2상을 진행 중이다.
한편 다국적 제약사들의 백신 개발 소식이 연이어 나오는 가운데 국내 기업들이 개발하는 코로나19 백신은 아직 임상 1상에 머물러 있다. 제넥신은 지난 6월 임상 1/2a상을 개시했고, 임상 1상 투약을 완료했으며 연내 임상 2상에 착수할 예정이다. 지난달 23일 식약처에서 임상 1상을 승인받은 SK바이오사이언스는 2일 서울대병원과 업무협약을 맺고 본격적인 백신 임상에 착수했다.

!['20년 째 공회전' 허울 뿐인 아시아 금융허브의 꿈 [외국 금융사 脫코리아]](https://img.etoday.co.kr/crop/140/88/2100022.jpg)
![[단독]"한 번 뗄 때마다 수 백만원 수령 가능" 가짜 용종 보험사기 기승](https://img.etoday.co.kr/crop/140/88/2100020.jpg)
![8만 달러 터치한 비트코인, 연내 '10만 달러'도 넘보나 [Bit코인]](https://img.etoday.co.kr/crop/140/88/2100256.jpg)

![환자복도 없던 우즈베크에 ‘한국식 병원’ 우뚝…“사람 살리는 병원” [르포]](https://img.etoday.co.kr/crop/140/88/2099863.jpg)






![불 꺼진 복도 따라 ‘16인실’ 입원병동…우즈베크 부하라 시립병원 [가보니]](https://img.etoday.co.kr/crop/85/60/2099872.jpg)
![[BioS]한미약품, 11일 기관투자자 대상 기업설명회 열어](https://img.etoday.co.kr/crop/85/60/2100453.jpg)






![“과립·멸균 생산, 독보적 노하우”...‘단백질 1등’ 만든 일동후디스 춘천공장 [르포]](https://img.etoday.co.kr/crop/85/60/2099348.jpg)
![[정치대학]이재명, 정치운명 가를 ‘운명의 주’…시나리오별 파장은?](https://img.etoday.co.kr/crop/300/170/2100294.jpg)
![오세훈 서울시장, 제7회 AI·드론봇 전투발전 콘퍼런스 [포토]](https://img.etoday.co.kr/crop/300/190/2100458.jpg)