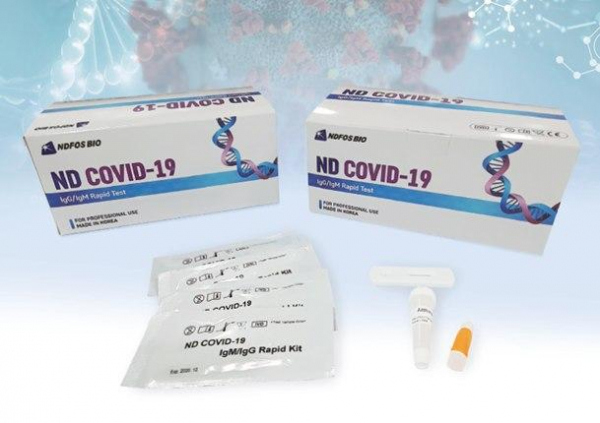
앤디포스의 코로나19 항체 신속 진단키트가 식품의약품안전처로부터 수출 품목 허가를 받았다.
앤디포스는 식품의약품안전처로부터 코로나19 항체 신속 진단키트 ‘ND COVID-19 IgG/IgM Rapid Test’의 수출 허가를 획득했다고 21일 밝혔다. 향후 앤디포스는 미국 FDA 긴급사용승인도 추진할 계획이다.
이번에 허가받은 신속 진단키트는 면역분석법을 이용해 혈액 내 존재하는 코로나19 특이 항체 유무를 검사하는 진단키트다.
앤디포스는 이번 진단키트의 주요 원재료인 COVID-19 항원을 기존 대장균보다 고등 생물인 곤충 세포에서 분리 정제한 것을 적용해 더욱 높은 정확도를 확보했다. 이번 수출 허가 과정 중 진행된 임상 시험 결과 95% 이상의 정확도를 보였다.
항체진단은 대규모 장비를 필요로 하는 분자진단과 달리 장소와 숙련도 등에 따른 제약이 없고 10분 이내 감염 여부를 확인할 수 있어 방역 인프라가 상대적으로 열악한 국가들을 중심으로 수요가 증가하고 있다.
앤디포스 관계자는 “앤디포스의 항체 신속 진단 키트는 타제품 대비 정확성과 편의성이 우수해 중남미, 중동, 아시아 등 각국에서 선주문이 잇따르고 있다”며 “이미 국내외 다수 업체와 공급 협상을 진행 중이다”고 말했다.
이어 “특히 지난 3일 유럽 CE 인증으로 이탈리아와 프랑스 등 유럽에서 테스트 물량 주문이 쇄도하고 있다“며 “향후 사내이사인 로져 콘버그 스탠포드 대학교수와 협업해 미국 FDA 긴급사용승인을 추진하고 미국 시장까지 수출을 확대할 예정”이라고 설명했다.
앤디포스는 기존에 수출허가를 획득한 코로나19 분자 진단키트와 항체 신속 진단키트뿐 아니라, 항원 신속 진단키트까지 개발을 완료해 코로나19 진단키트 관련 모든 기술력을 보유 중이다.

![다 상술인건 알지만…"OO데이 그냥 넘어가긴 아쉬워" [데이터클립]](https://img.etoday.co.kr/crop/140/88/2102336.jpg)
![‘2025 수능 수험표’ 들고 어디 갈까?…수험생 할인 총정리 [그래픽 스토리]](https://img.etoday.co.kr/crop/140/88/2102319.jpg)















![[채권뷰] 클래스원 제1차, 사모 이표채 표면금리 4.28%에 50억원 발행](https://img.etoday.co.kr/crop/85/60/2102537.jpg)
![[채권뷰] 교보생명보험 신종자본증권 수익률 4.60%에 1414억원 거래](https://img.etoday.co.kr/crop/85/60/2102538.jpg)

![다 상술인건 알지만…"OO데이 그냥 넘어가긴 아쉬워" [데이터클립]](https://img.etoday.co.kr/crop/300/170/2102336.jpg)
!['수능 끝, 홀가분해요' [포토]](https://img.etoday.co.kr/crop/300/190/2102419.jpg)