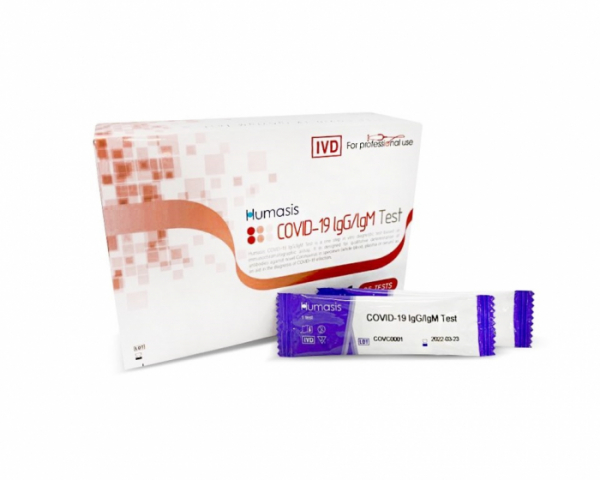
휴마시스는 지난 20일 자사 항체진단키트(Humasis COVID-19 IgG/IgM Test)가 FDA에 제품 등록됐다고 23일 밝혔다.
미국 내 신종코로나바이러스 진단 제품을 공급하기 위한 방법에는 미 FDA에 제품을 등록(NOTIFICATION PATH)하거나 긴급사용승인(EUA PATH)을 받는 두 가지의 경우가 있다. 신종코로나바이러스의 확진법으로 사용되는 RT-PCR 진단시약의 경우 단독진단으로 긴급사용승인을 받아야 한다. 이와 다르게 항체진단키트의 경우 제품 등록만으로도 미국 내 제품을 공급하는 것이 가능하다.
휴마시스의 제품은 체내 침투한 바이러스에 대응해 형성된 항체를 진단하는 방식의 항체진단키트로 이번 제품 등록을 통해 미국 내 수요를 빠르게 충족시킬 수 있게 됐다.
휴마시스는 미국의 코로나사태가 심화되던 지난 달부터 다수의 미국 기업으로부터 공급요청을 받아왔다. 이에 뉴욕, 펜실베니아, 플로리다, 텍사스, 캘리포니아 주 내 의료기관들에 제품 공급을 위한 계약 협의 중이며, 이번 FDA 제품 등록으로 계약 협의에 속도가 붙을 전망이다.
앞서 회사는 주한인도대사관과 체결한 코로나19 항체진단키트 50만 테스트 공급 계약을 비롯해 브라질 상파울루 지역에 국내 브랜드 최초 공급계약 등 다수의 해외 수출 계약을 맺고 공급을 진행해왔다. 이미 계약과 판매가 진행중인 국가는 브라질, 독일, 영국, 프랑스 등 30개 국이며 해외로 공급되는 물량은 약 300만 테스트 가량이다.
회사는 이미 계약이 체결된 다른 국가들의 납품 일정에 맞춰 순차적으로 미국 내 계약 및 납품을 진행할 계획이다.
차정학 휴마시스 대표는 “미국 주정부 5곳과 수출협의 중에 있으며, 제품 등록이 완료됨에 따라 계약이 성사될 가능성이 높아지고 있다”며 “현재 원활한 납품을 위해 생산능력을 최대치로 올려 공장을 가동하고 있고 이미 출하된 제품이 현지에서 성능을 인정 받고 있는 만큼, 추가 물량 요청에 대비하고 있다”고 전했다.

![부동산 PF 체질 개선 나선다…PF 자기자본비율 상향·사업성 평가 강화 [종합]](https://img.etoday.co.kr/crop/140/88/2101720.jpg)
![‘2025 수능 수험표’ 들고 어디 갈까?…수험생 할인 총정리 [그래픽 스토리]](https://img.etoday.co.kr/crop/140/88/2102319.jpg)
![전기차 수준 더 높아졌다…상품성으로 캐즘 정면돌파 [2024 스마트EV]](https://img.etoday.co.kr/crop/140/88/2102282.jpg)
![낮은 금리로 보증금과 월세 대출, '청년전용 보증부월세대출' [십분청년백서]](https://img.etoday.co.kr/crop/140/88/2102283.jpg)
![[종합] ‘공직선거법 위반’ 김혜경 벌금 150만원…法 “공정성·투명성 해할 위험”](https://img.etoday.co.kr/crop/140/88/2102280.jpg)
![이혼에 안타까운 사망까지...올해도 연예계 뒤흔든 '11월 괴담' [이슈크래커]](https://img.etoday.co.kr/crop/140/88/2101314.jpg)
!["늦었다고 생각할 때가 제일 빠를 때죠" 83세 임태수 할머니의 수능 도전 [포토로그]](https://img.etoday.co.kr/crop/140/88/2101767.jpg)














![‘2025 수능 수험표’ 들고 어디 갈까?…수험생 할인 총정리 [그래픽 스토리]](https://img.etoday.co.kr/crop/300/170/2102319.jpg)
!['수능 끝, 홀가분해요' [포토]](https://img.etoday.co.kr/crop/300/190/2102419.jpg)